Main Content
Nanobiologie: Lebenszeichen im Nanobereich
Wir erforschen Grundprinzipien und funktionale Beziehungen zwischen Molekularmechanik, Selektivität und Transport in biologischen Systemen.
Die Natur hat komplexe biologische Maschinen geschaffen - faszinierend und technologisch unerreicht. Wir setzen quantitative Techniken der Nanowissenschaften ein und entwickeln neue biophysikalische Methoden, um die Interaktionen zu erforschen, die hinter der biologischen Funktionalität stehen. Im Gegenzug realisieren und implementieren wir biomimetische Konzepte für innovative nicht-physiologische Anwendungen.
Selektiver Transport durch den Kernporenkomplex
Uns interessiert, wie der Kernporenkomplex (NPC) den schnellen, selektiven Austausch spezifischer Cargo-Proteine zwischen Zytoplasma und Zellkern ermöglicht. Jede Kernpore mit einem Durchmesser von 50 nm fungiert als "Schleuse", die sich öffnet oder schliesst, je nachdem, ob es die "Identität" seines molekularen "Gastes" erkennt. Wir wollen die biophysikalischen Mechanismen der NPC-Transportselektivität entschlüsseln - ein wichtiges Vorhaben, denn Viren machen sich beim Eindringen in den Zellkern die gleichen Mechanismen zunutze.
Mechanobiologie und Krankheitsdiagnostik
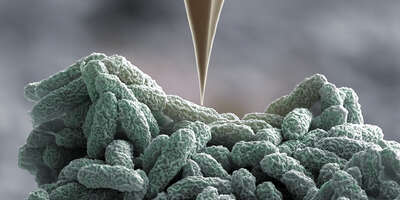
Anhand der in unserem Labor entwickelten Rasterkraftmikroskop-Technologien erforschen wir die Mechanobiologie von Zellen in Geweben mit Sub-Nanonewton-Präzision. Wir gehen davon aus, dass man mithilfe solcher Informationen Erkrankungen wie Brustkrebs und Knorpeldegeneration (Arthrose) detektieren kann.
Von der Natur inspiriert: biomimetische Strategien
Der Begriff "Protein-Targeting" bezeichnet den Transport von Proteinen zu bestimmten Zielorten innerhalb der biologisch komplexen Zelle. Wir wollen diese biochemische Selektivität und die Protein-Targeting-Steuerung in biomimetischen molekularen Transportsystemen nachbilden. Ein potenzieller Einsatz in der Wasseraufbereitung und bei Bioseparationen ist denkbar.